
Pages perso de
Fred PLACIN
menu
>mon CV
>mes postdoc
>au Japon
>Rhodia
>Colas
>ma thèse
Plan du site
visiteurs
Organogel de 2,3-dialcoxyanthracènes et composés apparentés, structures et propriétés
Thèse de doctorat de lUniversité Bordeaux I
Specialité : Chimie-physique
Directeurs de recherche : Jean-Pierre
Desvergne, directeur de recherche au CNRS
Jean-Claude Lassègues,
directeur de recherche au CNRS
Lieu : Laboratoire de Chimie Organique et Organométallique
UMR 5802
Laboratoire de Physico-Chimie Moléculaire UMR 5803
351, cours de la Libération
33405 Talence cedex
soutenue le 6 octobre 1999
Commission dexamen : Y.Gnanou (président), F. Cansell,
J.-P. Desvergne,
J.-C. Lassègues, J. Delaire (Rapporteur), P. Terech (Rapporteur),
Introduction
Les propriétés gélifiantes du DDOA (2,3-didécyloxanthracène),
petite molécule aromatique (M=490 g/mol) ne comportant pas de liaisons
hydrogènes, ont été découvertes au laboratoire
en 1989. Ce composé fluorescent peut à très basse
concentration gélifier les solvants organiques. Grâce à
deux approches complémentaires, jai pu proposer durant ma thèse,
des hypothèses sur l'origine moléculaire de leurs propriétés
gélifiantes et un modèle décrivant l'organisation
microscopique dans les gels.
DDOA |
Etudes physicochimiques des gels de DDOA
Une première approche donne une description détaillée
de la structure et des propriétés des gels (gels physiques)
de DDOA obtenus avec divers solvants organiques.
Il est montré que l'agrégation des molécules de
DDOA en fibres d'une centaine de nanomètres de diamètre est
à l'origine de la formation d'un réseau 3D qui bloque l'écoulement
des liquides. Les températures de gel et de dégel de solutions
de DDOA dans des solvants organiques ont été déterminées
à l'aide d'une méthode de diffusion de la lumière
que jai mise au point au laboratoire, le milieu gélifié
étant particulièrement opaque. La transition solution-gel
est une transition de phase dordre 1, les températures de gels
et de dégel suivent une loi de variation inversement proportionnelle
au logarithme de la fraction molaire du soluté. Les paramètres
thermodynamiques de la transition sol gel ont été calculés
 |
Graphes ln(f) = f(1/T) obtenus lors du gel du système
DDOA / carbonate de propylène
|
Le DDOA peut gélifier de nombreux fluides comme les solvants
organiques, les cristaux liquides, les électrolytes et les fluides
supercritiques:
- La gélification de milieux mésogènes orientés
donne lieu à la formation dun réseau de fibres orientées
à 60 degrés par rapport à lalignement du cristal
liquide, ces travaux doivent être prochainement approfondis.
- Les électrolytes gélifiés présentent
une aussi bonne conductivité ionique que lélectrolyte liquide
correspondant, ainsi qu'une stabilité électrochimique acceptable.
La réalisation de supercondensateurs gélifiés par
le DDOA a été étudiée.
- La désolvatation des gels (déthanol) ou la gélification
du CO2 par voie supercritique donne des aérogels d'une densité
extrêmement faible (2 mg/cm3). Ces aérogels se sont révélés
être dexcellents matériaux pour létude structurale
des fibres de DDOA. De plus des applications intéressantes peuvent
être envisagées comme lutilisation de ces aérogels
pour le piégeage de particule, comme support de catalyseur ou encore
comme nanodétecteur de fluorescence. A ma connaissance, ce sont
les premiers aérogels physiques organiques synthétisés
à ce jour par voie supercritique.
 |
 |
Les études spectroscopiques IR, UV, fluorescence, Raman, associées
à la diffraction RX, et à la microscopie électronique
ont permis de proposer un arrangement des molécules de DDOA dans
les fibres du gel et un mécanisme pour la formation de ces fibres
:
- Lobservation de gel en microscopie électronique, notamment
par la technique du fond noir, démontre que les fibres du gel ne
sont pas cristallines, un arrangement cylindrique étant fortement
probable vu la géométrie de lédifice.
- Lanalogie spectrale entre le DDOA et son analogue cristalisé
avec des chaînes à 6 carbones, le 2,3-didecyloxyanthracène
(DHOA), indique que les molécules de DDOA sorganisent sous forme
de couches au sein du gel. En effet, le DHOA peut à la fois donner
un gel et cristalliser. La diffraction des RX sur un cristal de DHOA montre
un arrangement moléculaire sous forme de plan.
- Des mesures de dichroisme linéaire en microscopie IR et en
fluorescence sur des fibres daérogel orientées ont été
réalisées. Le fort effet dichroique observé sur la
majeure partie des fréquences infrarouges à permis de positionner
chaque partie de la molécule de DDOA par rapport a laxe de la fibre.
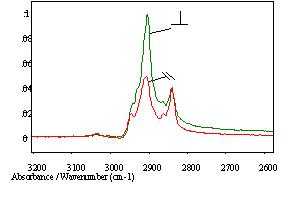
Spectre infrarouge du DDOA polarisé parallèlement et perpendiculairement par rapport à laxe dune fibre. |
Dautres forts effets dichroiques sont observables sur les autres fréquences infrarouges du DDOA
Ces observations ont permis de proposer un arrangement moléculaire
fortement probable des molécules de DDOA dans les fibres mais aussi
démettre une hypothèse sur le mécanisme de formation
de ces fibres.
Synthèse et études de composés apparentés au DDOA
La seconde approche décrit la synthèse et les propriétés
gélifiantes de divers composés apparentés au DDOA.
Outre les anthraquinones et les phénazines synthétisés
au laboratoire, létude des composés issus de lhydrogénation
catalytique du DDOA (dihydroDDOA et tétrahydroDDOA) a permis
de montrer limportance de la planéite du coeur aromatique de la
molécule dans le processus de gélification : en effet, le
dihydroDDOA qui présente une partie cyclique biaisée est
un mauvais gélifiant alors que le tétrahydroDDOA, aussi bon
gélifiant que le DDOA, à ces trois cycles relativement plans.
Dautre part, des composés à quatre cycles peuvent eux aussi
gélifier les solvants organiques. Cest le cas des 2,3-dialcoxy-5,12-diazatétracènes,
composés de couleur orangée, capables de former des gels
stables à plus de 100º et présentants des propriétés
acidochromiques intéressantes. De plus la synthèse de ces
composés se fait en seulement deux étapes contre 7 pour le
DDOA.

2,3-didécyloxy-5,6,7,8-tétrahydroanthracène(TétrahydroDDOA) |
2,3-didécyloxy-9,10-dihydroanthracène(DihydroDDOA) |

2,3-dialcoxy-5,12-diazatétracènes |
forme moleculaire |
La forme moléculaire spécifique des ces composés
semble être primordiale pour obtenir des propriétés
gélifiantes. Néanmoins, une interaction électronique
particulière pourrait aussi être à lorigine de la
gélification puisque le composé diazaanthracénique
analogue au DDOA ne forme pas de gel, les deux azotes modifiant la répartition
électronique au sein du noyau aromatique.

2,3-dialcoxy-1,4-diazaanthracènes |
Conclusion
Le processus de gélification fait appel à un mécanisme
complexe avec un équilibre subtil entre la forme moléculaire
et les interactions de Van der Waals liants deux molécules. Néanmoins,
ce travail a permis de mieux comprendre ces systèmes ; les avances
significatives ayant été faites dans la détermination
de lédifice moléculaire des gels, dans la réalisation
par voie supercritique daérogels très prometteurs et dans
la synthèse de nouveaux composés gélifiants.
Publications issues de ces travaux
1. A New Example of Small Molecular Non-Hydrogen Bonding Gelators for Organic Solvents.
F. Placin, M. Colomes et J.-P. Desvergne
Tetrahedron Letters, 1997, 38, 2665-2668.
2. Organic low molecular weight aerogel formed in supercritical fluids
F. Placin, J.P. Desvergne, F. Cansell
Journal of Materials Chemistry, 2000, 10, 2147-2149
3. New organogelators based on linear azapolycyclic arenes
F. Placin, G. Clavier, F. Najera, J.P. Desvergne, J.L. Pozzo
polycyclic aromatic compounds
4. Organogel Electrolytes Based on a Low Molecular Weight Gelator :
2,3-Bis(n-decyloxy)antracene
F. Placin, J.P. Desvergne, J.C. Lassegues
Chemistry of. Materials, 2001, 13, 117 -121
5. Molecular arrangement in the gel fibers of 2,3-didecyloxyanthracene (DDOA) : a spectroscopic and theoretical approach
F. Placin, J.P. Desvergne, J.C. Lassegues, C. Belin, T. Buffeteau, B. Desbats, L. Ducasse.
Langmuir ; 2003; 19(11) pp 4563 - 4572
